tính khối lượng oxi cần dùng là trong phòng thhis nghiệm khi đốt cháy sắt ở nhiệt độ cao thu đc 4,64 oxit sắt từ (Fe304)
Tính khối lượng oxi cần dùng trong phòng thí nghiệm, khí đốt cháy sắt ở nhiệt độ cao thu thu được 4,64g oxit sắt từ (Fe3O4)
n Fe3O4=\(\dfrac{4,64}{232}=0,02mol\)
3Fe+2O2-to>Fe3O4
0,06----0,04---0,02
=>m O2=0,04.32=1,28g
\(n_{Fe_3O_4}=\dfrac{m}{M}=\dfrac{4,64}{232}=0,02mol\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
0,06 0,02 ( mol )
\(m_{Fe}=n_{Fe}.M_{Fe}=0,06.56=3,36g\)
nFe3O4=4,64/232=0,02(mol)
PTHH: 3Fe+2O2 to⟶Fe3O4
0,06 mol ← 0,02 mol
mFe=56×0,06=3,36(g)
mO2=4,64–3,36=1,28(g)
Chúc em học giỏi
Khi đốt cháy sắt trong oxi ở nhiệt độ cao, thu được oxit sắt từ. Để điều chế 4,64 gam oxit sắt từ thì khối lượng oxi đem dùng là *
1,28 gam.
3,24 gam.
4,56 gam.
2,25 gam.
\(n_{Fe_3O_4}=\dfrac{4,64}{232}=0,02\left(mol\right)\)
3Fe + 2O2 \(\underrightarrow{t^o}\) Fe3O4
0,04 0,02 ( mol )
\(m_{O_2}=0,04.32=1,28\left(g\right)\)
=> Đáp án A
Khi đốt cháy sắt trong oxi ở nhiệt độ cao, thu được oxit sắt từ. Để điều chế 4,64 gam oxit sắt từ thì khối lượng oxi đem dùng là *
1,28 gam.
3,24 gam.
4,56 gam.
2,25 gam.
Trong phòng thí nghiệm,người ta điều chế oxit sắt từ bằng cách dùng Oxi oxi hóa Sắt ở nhiệt độ cao
a)Tính thành phần%theo khối lượng của nguyên tố Sắt có trong oxi sắt từ
b) Tính số gam không khí Oxi cần dùng để điều chế được 4,64 g oxit sắt từ?
c)Để điều chế được lượng Oxi nói trên cần phân hủy bao nhiêu gam KMnO4 (coi như không có sự hao hụt trong quá trình điều chế ) ?
(Cho Fe = 56;O=16;K=39;Mn=55)
a.\(\%Fe=\dfrac{56.3}{56.3+16.4}.100=72,41\%\)
b.\(n_{Fe_3O_4}=\dfrac{4,64}{232}=0,02mol\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
0,04 0,02 ( mol )
\(m_{O_2}=0,04.32=1,28g\)
c.\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,08 0,04 ( mol )
\(m_{KMnO_4}=0,08.158=12,64g\)
a, Ta có: \(n_{Fe_3O_4}=\dfrac{4,64}{232}=0,02\left(mol\right)\)
PT: \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
THeo PT: \(n_{O_2}=2n_{Fe_3O_4}=0,04\left(mol\right)\Rightarrow V_{O_2}=0,04.22,4=0,896\left(l\right)\)
b, PT: \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
\(n_{KMnO_4}=2n_{O_2}=0,08\left(mol\right)\Rightarrow m_{KMnO_4}=0,08.158=12,64\left(g\right)\)
a) \(n_{Fe_3O_4}=\dfrac{m_{Fe_3O_4}}{M_{Fe_3O_4}}=\dfrac{4,64}{232}=0,02\left(mol\right)\).
PTHH : \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
Mol : 3 : 2 : 1
Mol 0,04 ← 0,02
\(\Rightarrow V_{O_2}=n_{O_2}.22,4=\left(0,04\right).\left(22,4\right)=0,896\left(l\right)\).
b) Từ phương trình ở câu a \(\Rightarrow n_{O_2}=0,04\left(mol\right)\).
PTHH : \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
Mol : 2 : 1 : 1 : 1
Mol : 0,08 ← 0,04
\(\Rightarrow m_{KMnO_4}=n_{KMnO_4}.M_{KMnO_4}=\left(0,08\right).158=12,64\left(g\right)\).
4. Khi đốt cháy sắt trong oxi ở nhiệt độ cao thu được oxit sắt từ Fe3O4. a) Tính khối lượng sắt và thể tích khí oxi (đktc) cần dùng để điều chế được 6,96 gam Fe3O4 . b) Tính khối lượng kali clorat KClO3 cần dùng để điều chế được lượng oxi dùng cho phản ứng trên.
a. \(n_{Fe_3O_4}=\dfrac{6,96}{232}=0,03\left(mol\right)\)
PTHH : 3Fe + 2O2 -to-> Fe3O4
0,09 0,06 0,03
\(m_{Fe}=0,09.56=5,04\left(g\right)\)
\(V_{O_2}=0,06.22,4=1,344\left(l\right)\)
b. PTHH : 2KCl + 3O2 -> 2KClO3
0,06 0,04
\(m_{KClO_3}=0,04.122,5=4,9\left(g\right)\)
4
n Fe3O4=\(\dfrac{6,96}{232}=0,03mol\)
3Fe+2O2-to>Fe3O4
0,09---0,06-----0,03 mol
=>m Fe=0,09.56=5,04g
=>VO2=0,06.22,4=1,344l
b)
2KClO3-to>2KCl+3O2
0,04----------------------0,06 mol
=>m KClO3=0,04.122,5=4,9g
\(n_{Fe_3O_4}=\dfrac{6,96}{232}=0,03\left(mol\right)\\ 3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\\ n_{Fe}=3.0,03=0,09\left(mol\right);n_{O_2}=0,03.2=0,06\left(mol\right)\\ a,\Rightarrow m_{Fe}=0,09.56=5,04\left(g\right);V_{O_2\left(đktc\right)}=0,06.22,4=1,344\left(l\right)\\ 2KClO_3\rightarrow\left(t^o\right)2KCl+3O_2\uparrow\\ n_{KClO_3}=\dfrac{2}{3}.n_{O_2}=\dfrac{2.0,06}{3}=0,04\left(mol\right)\\ \Rightarrow b,m_{KClO_3}=122,5.0,04=4,9\left(g\right)\)
Trong phòng thí nghiệm khi đốt cháy sắt trong oxi ở nhiệt độ cao được oxit sắt từ F e 3 O 4
Số gam kali pemanganat K M n O 4 cần dùng để điều chế lượng khí oxi cần dùng cho phản ứng trên là:
A.3,16g B. 9,48g C.5,24g D.6,32g
Hãy giải thích sự lựa chọn.
Theo câu a: số mol của O 2 : n O 2 = 0,02mol
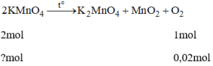
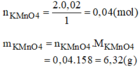
Đốt cháy hoàn toàn 3,36 gam sắt Fe ở nhiệt độ cao thu được oxit sắt từ Fe3O4.
a/ Tính khối lượng oxit sắt từ thu được sau phản ứng.
b/ Tính thề tích khí oxi cần dùng (đktc).
a) \(n_{Fe}=\dfrac{3,36}{56}=0,06\left(mol\right)\)
PTHH: 3Fe + 2O2 --to--> Fe3O4
0,06->0,04------->0,02
=> mFe3O4 = 0,02.232 = 4,64 (g)
b) VO2 = 0,04.22,4 = 0,896 (l)
Trong phòng thí nghiệm khi đốt cháy sắt trong oxi ở nhiệt độ cao được oxit sắt từ F e 3 O 4
Số gam sắt và khí oxi cần dùng điều chế 2,32g oxit sắt từ lần lượt là:
A. 0,84g và 0,32g B. 2,52g và 0,96g
C. 1,86g và 0,64g D. 0,95g và 0,74g
Hãy giải thích sự lựa chọn.
trong phòng thí nghiệm để điều chế sắt từ oxit ngta đốt cháy sắt trong khí oxintinh1 khối lượng sắt và khí oxi cần dùng để điều chế đc 4.64g sat71 từ oxi
\(n_{Fe_3O_4}=\dfrac{m_{Fe_3O_4}}{M_{Fe_3O_4}}=\dfrac{4,64}{232}=0,02mol\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
0,06 0,04 0,02 ( mol )
\(m_{Fe}=n_{Fe}.M_{Fe}=0,06.56=3,36g\)
\(m_{O_2}=n_{O_2}.M_{O_2}=0,04.32=1,28g\)
\(pthh:3Fe+2O_2\overset{t^o}{--->}Fe_3O_4\)
Ta có: \(n_{Fe_3O_4}=\dfrac{4,64}{232}=0,02\left(mol\right)\)
Theo pt: \(n_{Fe}=3.0,02=0,06\left(mol\right)\)
\(\Rightarrow m_{Fe}=0,06.56=3,36\left(g\right)\)
Theo pt: \(n_{O_2}=2.0,02=0,04\left(mol\right)\)
\(\Rightarrow m_{O_2}=0,04.32=1,28\left(g\right)\)